Kalziumeinstrom durch Plasma-Membran: Nanorupturen treiben Axon-Degeneration an
Ein deutsches Forscherteam identifizierte einen Mechanismus, der sich bei Multipler Sklerose (MS) auf die Degeneration der langen Nervenfortsätze, der sogenannten Axone, und somit auf das Ausmaß der bleibenden Behinderung auswirken kann.
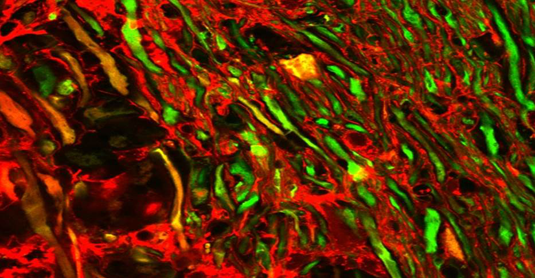
Prof. Dr. Martin Kerschensteiner und Prof. Dr. Thomas Misgeld identifizierten mit ihren Kolleginnen und Kollegen in einem Tiermodell der multiplen Sklerose zytoplasmatische Kalziumakkumulationen als Schlüsselmotor der Zerstörung von langen Nervenzellfortsätzen, sogenannten Axiomen. Im Fachmagazin Neuron beschreiben sie, dass winzige Risse in der Zellmembran einen Eintrittspfad für extrazelluläres Kalzium bieten, worauf sich Kalzium im Axoplasma ansammelt.
Axonverlust als Schlüsselfaktor für persistente Funktionsdefizite
Bei Menschen mit Multipler Sklerose bestimmt meist der Axonverlust, inwieweit eine dauerhafte Behinderung auftritt. In einer Mitteilung der Ludwig-Maximilians-Universität München schreiben die beteiligten Forschenden, dass bereits in früheren Studien beobachtet worden sei, dass Axone in der Nähe entzündlicher Läsionen häufig anschwellen und anschließend zugrunde gehen können, sich allerdings einige Axone spontan erholen und wieder abschwellen.
Kalzium-initiierte Axon-Degeneration
Anhand eines in-vivo Mikroskopie-Ansatzes zeigten die deutschen Forscherinnen und Forscher in einem Multiple-Sklerose-Modell, dass der zytoplasmatische Kalziumspiegel die Wahl zwischen dem Axonverlust und dem Überleben bestimmt. So führt ein erhöhter Kalziumspiegel zu einem hohen Risiko, anzuschwellen und geringen Chancen, sich von dem geschwollenen Zustand zu erholen. Dabei beginnen die Veränderungen in einem relativ frühen Stadium.
Mithilfe eines an ein Makrokmolekül gekoppelten Fluoreszenzfarbstoffs konnten sie nachweisen, dass überschüssiges Kalzium aus dem extrazellulären Raum stammt und durch winzige Risse in der Zellmembran in das Axon eindringt.
Das Ausmaß der bleibenden Behinderung von Menschen mit Multipler Sklerose hängt maßgeblich von der Degeneration der Axone ab. Durch winzige Risse in der Zellmembran kann schädliches Kalzium einströmen.
„Dass Risse in der Zellmembran auch im entzündeten Nervensystem zum Absterben vom Nervenfasern beitragen können, ist eine neue Erkenntnis, die in der Zukunft auch therapeutisch relevant sein könnte, erklärte Prof. Dr. Thomas Misgeld vom Institut für Neuronale Zellbiologie an der Technischen Universität München.
Da Nervenfasern bei Menschen mit Rückenmarksverletzungen durch mechanische Verletzungen entstandene Risse wieder heilen können, hoffen die Wissenschaftlerinnen und Wissenschaftler, dass ein besseres Verständnis der Entstehung und Reparatur der Risse ein wichtiger Schritt hin zu neuen therapeutischen Angriffszielen sein könnte.
Maarten E. Witte, Adrian-Minh Schumacher, Christoph F. Mahler, Jan P. Bewersdorf, Jonas Lehmitz, Alexander Scheiter, Paula Sánchez, Philip R. Williams, Oliver Griesbeck, Ronald Naumann, Thomas Misgeld und Martin Kerschensteiner: Calcium Influx through Plasma-Membrane Nanoruptures Drives Axon Degeneration in a Model of Multiple Sclerosis. Neuron 101, 1–10, February 20, 2019, DOI: https://doi.org/10.1016/j.neuron.2018.12.023
Marta M. Wesolowski: In vivo analysis of calcium-initiated axon degeneration in an animal model of MS. Dissertation der Graduate School of Systemic Neurosciences der Ludwig-Maximilians-Universität München, 2018
Quelle: Aussendung der Ludwig-Maximilians-Universität München
Wesentliche Ergebnisse
- Zytoplasmatische Kalziumakkumulationen sagen die Axon-Degeneration bei Neuroinflammation voraus.
- Die Freisetzung aus dem axoplasmatischen Retikulum erklärt nicht diese Kalziumansammlungen.
- Der Kalziumzufluss aus dem extrazellulären Raum treibt die Axon-Degeneration an.
- Bruchstellen im Nanomaßstab ermöglichen den Eintritt von Kalzium durch die axonale Plasmamembran.



